解:设纯铁5.6g能生成氢气的质量为x,则有
Fe+H2SO4=FeSO4+H2↑56 2
5.6g x

x=0.2g
设纯钠5.6g能生成氢气的质量为y,则有
2Na+H2SO4=Na2SO4+H2↑
46 2
5.6g y

y≈0.24g
设纯镁5.6g能生成氢气的质量为z,则有
Mg+H2SO4=MgSO4+H2↑
24 2
5.6g z

z≈0.47g
设纯铝5.6g能生成氢气的质量为a,则有
2Al+3H2SO4=Al2(SO4)3+3H2↑
54 6
5.6g a

a≈0.62g
设纯锌5.6g能生成氢气的质量为b,则有
Zn+H2SO4=ZnSO4+H2↑,
65 2
5.6g b
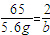
b≈0.17g
根据平均值法,若是铁与钠或镁或铝的混合物,则生成的氢气质量应该大于0.2g,不可能为0.195g,故混有的杂质是锌。
故选:D.
或者:
设该金属混合物为纯净金属M,其化合价为+2价,其相对原子质量为x.
M+H2SO4=MSO4+H2↑
x 2
5.6g 0.195g

x=57.4g
由于铁本身的相对原子质量为56,所以含有的杂质的相对原子质量大于57.4,所以含有的杂质为锌。
故选:D.
以上为百科题库网整理的关于"某含铁样品5.6g与足量稀硫酸完全反应后产生氢气0.195g,则其所含杂质可能是( )"试题答案及解析,如想学习更多化学类竞赛题,欢迎访问www.baiketk.com查看搜索更多相关信息。
转载请注明:百科题库网https://www.baiketk.com/q_o6087b16407992.html